Hvordan elektricitet ledes gennem væsker
Elektricitet og væsker er en livsfarlig kombination, som folk undgår. Processen, hvor en elektrisk strøm passerer gennem en væske, kaldes elektrolyse. Lær mere om, hvordan elektricitet ledes gennem væsker med denne korte guide.
Hvad kaldes ledende væsker?
Ledende væsker er kendt som elektrolytter. Elektrolytter er stoffer, der indeholder frie ioner og kan lede elektricitet, når de opløses i vand eller et andet opløsningsmiddel. Der findes to hovedtyper af elektrolytter:
- Stærke elektrolytter: Dette er stoffer, der dissocieres fuldstændigt til ioner i opløsning, hvilket resulterer i høj ledningsevne. Eksempler er salte som natriumklorid (bordsalt), syrer som saltsyre og baser som natriumhydroxid.
- Svage elektrolytter: Disse dissocieres delvist til ioner i opløsning, hvilket fører til lavere ledningsevne sammenlignet med stærke elektrolytter. Eksempler er eddikesyre (findes i eddike) og ammoniak.
Elektrolytter spiller en afgørende rolle i forskellige industrielle processer, biologiske funktioner og dagligdags anvendelser. De er f.eks. vigtige i batterier, hvor de letter strømmen, og i menneskekroppen, hvor de hjælper med at regulere nerve- og muskelfunktionen.
Vand
Vand kan være ledende, men er det ikke altid. Destilleret vand indeholder ingen ioner og er ikke ledende. Rent vand indeholder meget få ioner, så det er en dårlig elektrisk leder. Vand fra hanen indeholder ofte salt eller andre urenheder, som tilfører ioner til vandet og gør det ledende.
Det er derfor, det er farligt at røre ved stik eller stikkontakter med hænder, der er våde af vand fra hanen. Elektriciteten vil bevæge sig gennem væsken og kan give personen stød.
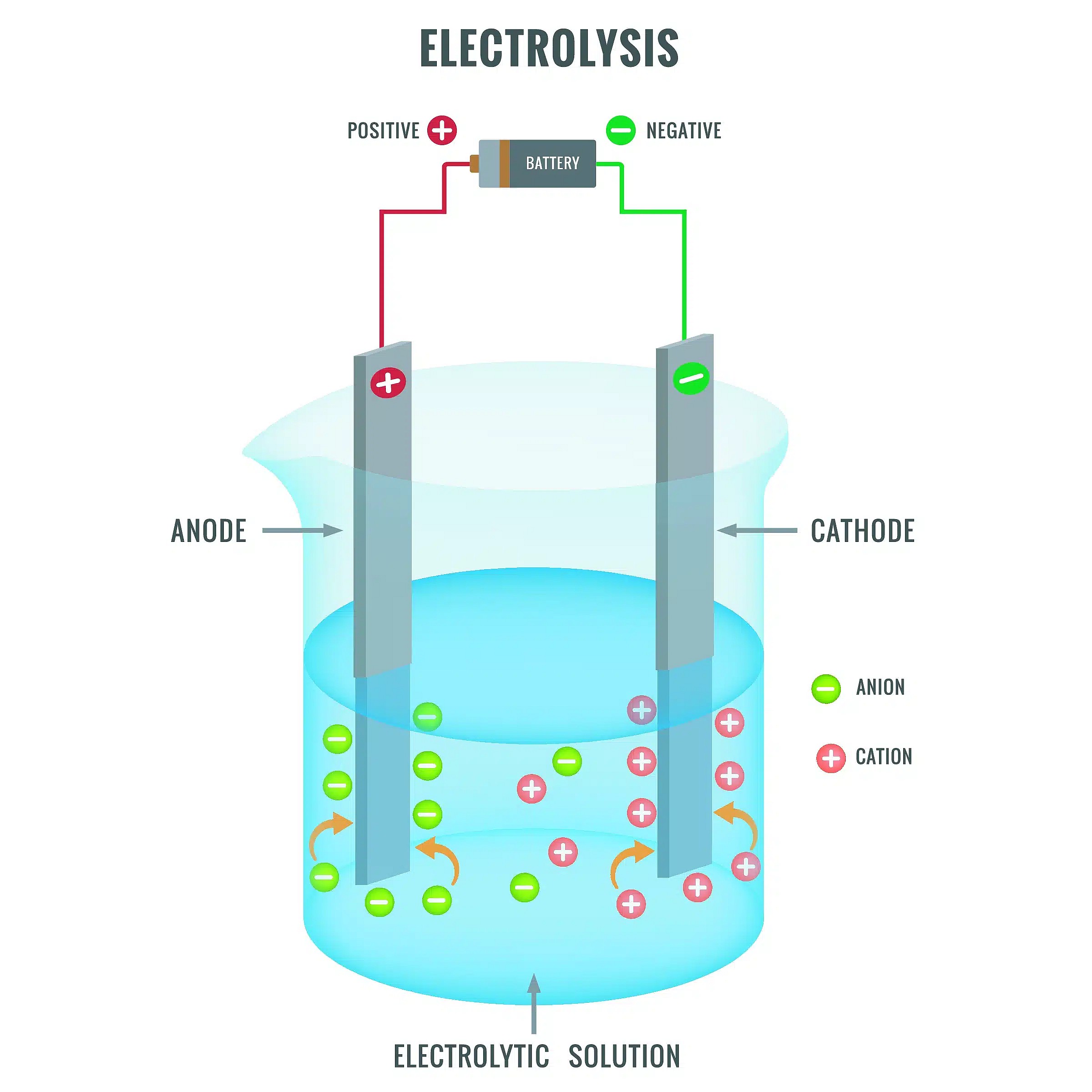
Elektrolyse
Elektrolyse er en kemisk proces, der bruger en elektrisk strøm til at drive en ikke-spontan kemisk reaktion. Denne proces er meget udbredt i forskellige industrielle og videnskabelige anvendelser. Under elektrolyse sendes en elektrisk strøm gennem en elektrolyt, hvilket får ionerne i elektrolytten til at bevæge sig mod elektroderne, hvor de gennemgår kemiske reaktioner.
Sådan virker elektrolyse
- Elektrolyt: Det stof, der leder elektricitet og gennemgår kemiske ændringer under elektrolyse. Det kan være en væske eller en opløsning, der indeholder ioner.
- Elektroder: To ledende materialer, typisk lavet af metal eller grafit, placeres i elektrolytten. Den positive elektrode kaldes anoden, og den negative elektrode kaldes katoden.
- Elektrisk strøm: En strømkilde, som f.eks. et batteri eller en strømforsyning, leverer den elektriske strøm, der driver elektrolyseprocessen.
Når den elektriske strøm løber gennem elektrolytten, får den de positive ioner (kationer) til at bevæge sig mod katoden, hvor de får elektroner (reduktion), og de negative ioner (anioner) til at bevæge sig mod anoden, hvor de mister elektroner (oxidation). Denne bevægelse af ioner og de deraf følgende kemiske reaktioner er grundlaget for elektrolyse.
Anvendelser af elektrolyse
Elektrolyse har mange praktiske anvendelser, bl.a:
- Galvanisering: Belægning af en metalgenstand med et tyndt lag af et andet metal for at forbedre dens udseende, korrosionsbestandighed eller andre egenskaber.
- Elektroraffinering: Rensning af metaller ved at fjerne urenheder gennem elektrolyse.
- Elektrolyse af vand: Spaltning af vand til brint- og iltgasser, som kan bruges som rene energikilder.
- Elektrolyse i vandbehandling: Fjerner forurenende stoffer fra vand ved at nedbryde dem til mindre skadelige stoffer.
Betydningen af elektrolyse
Elektrolyse er vigtig i forskellige industrier, herunder fremstilling, energiproduktion og miljøbeskyttelse. Den muliggør blandt andet produktion af metaller med høj renhed, produktion af brintbrændstof og rensning af spildevand. At forstå principperne og anvendelserne af elektrolyse er afgørende for at fremme teknologien og forbedre de industrielle processer.
Ikke-ledende væsker
Væsker, der ikke er ledende, tillader ikke elektricitet at strømme gennem dem. Disse væsker har kun få eller ingen ioner i sig. Elektricitet ledes gennem væsker via ioner, og uden dem kan elektriciteten ikke bevæge sig gennem væsken.
Væskers ledningsevne kan variere, og de bliver mere ledende, jo flere ioner der er. Elektrolyse er en proces, der udføres med vilje for at hjælpe med at belægge metaller, såsom forsølvning, med et andet stof. Det bruges også til at udvinde eller rense nogle metaller - f.eks. raffinering af kobber ved elektrolyse og udvinding af aluminium.
For mere information om farerne ved elektricitet, der passerer gennem væsker, eller for professionelle elektriske konsulenttjenester Kontakt Dreiym Engineering i dag.